Cancer Cell:南方医科大学董忠谊团队破解放射免疫治疗远端效应受限的机制
来源:生物世界 2025-03-18 09:50
该研究阐明了放射免疫治疗中远端效应受限的机制,首次揭示 PAI-1/SFRP2 信号轴通过周细胞-CAF转化调控远端效应,填补了放射免疫治疗中基质细胞作用机制的空白。
南方医科大学南方医院董忠谊、吴德华、白雪、官键等人在 Cell 子刊 Cancer Cell 上发表了题为:PAI-1-driven SFRP2high cancer-associated fibroblasts hijack the abscopal effect of radioimmunotherapy 的研究论文。
该研究阐明了放射免疫治疗中远端效应受限的机制,首次揭示了 PAI-1 驱动高表达SFRP2的癌症相关成纤维细胞劫持放射免疫治疗的远端效应的机制,填补了放射免疫治疗中基质细胞作用机制的空白,为改善实体瘤免疫治疗效果提供了新靶点和新思路。

在这项最新研究中,研究团队通过全基因组 CRISPR 筛选,发现了 SFRP2 在癌症相关成纤维细胞(CAF)中高表达,且在放射免疫治疗后未辐射的肿瘤中显著上调。SFRP2 高表达的癌相关成纤维细胞(SFRP2high CAF)通过重塑血管周围免疫抑制微环境,抑制 CD8+ T细胞浸润,从而阻碍远端效应。
基因敲除或药物阻断 SFRP2,可显著增强 CD8+ T细胞招募,改善未辐射肿瘤的免疫微环境,促进远端效应。
接下来,研究团队通过血清蛋白质组学揭示,经辐射的肿瘤会分泌的 PAI-1,通过血液循环到达远端肿瘤,进而通过 LRP1/p65 信号轴触发远处肿瘤周细胞向 SFRP2high CAF 的细胞命运转变,形成免疫抑制性的血管周围微环境。
在这些发现的基础上,研究团队发现,使用 SFRP2 中和抗体或 PAI-1 抑制剂(PAI-039)可逆转 CAF 的免疫抑制功能,显著增强放射免疫治疗的远端效应。在患者来源的异种移植(PDX)小鼠模型中,靶向 SFRP2 或 PAI-1,有效激活了未辐射肿瘤的免疫应答,验证了该发现的临床转化潜力。
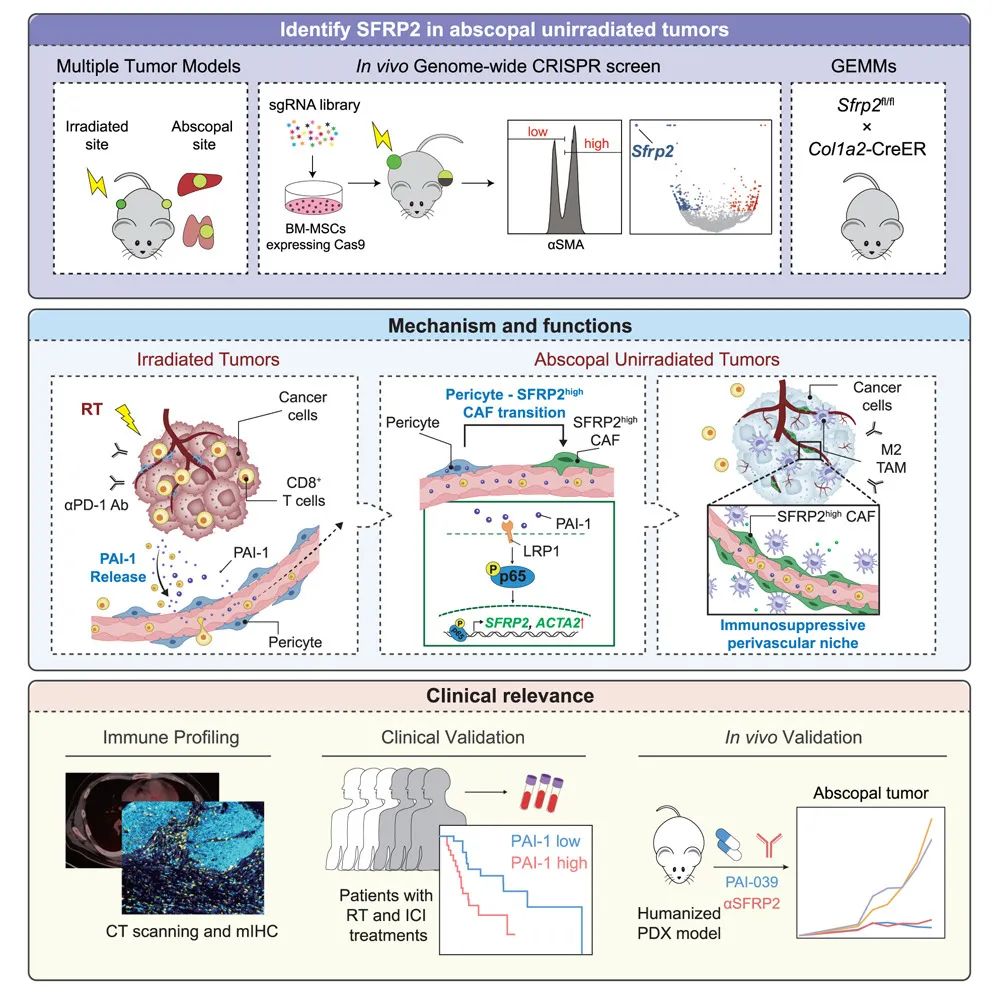
该研究阐明了放射免疫治疗中远端效应受限的机制,首次揭示 PAI-1/SFRP2 信号轴通过周细胞-CAF转化调控远端效应,填补了放射免疫治疗中基质细胞作用机制的空白。该研究还表明了基线 CD8+ T细胞浸润水平和 PAI-1 表达可作为预测远端效应的潜在标志物,为改善实体瘤免疫治疗效果提供了新靶点和新思路。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


